近日我校电子工程与光电技术学院陈钱、左超教授课题组提出了一种全新的无标记、高通量“明暗场混合光强传输”(HBDTI)定量相位成像技术。研究成果以“Hybrid brightfield and darkfield transport of intensity approach for high-throughput quantitative phase microscopy”(用于高通量定量相位显微成像的明暗场混合光强传输方法)为题发表于光学领域顶级期刊Advanced Photonics(先进光子学)。我校博士生卢林芃与博士后李加基为本文的共同第一作者,我校左超教授、陈钱教授与香港大学的Edmund Y. Lam教授为论文的共同通讯作者。文章链接:https://doi.org/10.1117/1.AP.4.5.056002。
研究团队所提出的明暗场混合光强传输技术(hybrid brightfield and darkfield transport of intensity,HBDTI)是一种全新的无标记、高通量定量相位成像技术。与仅使用明场照明的传统光强传输方程(TIE)相位恢复方法相比,HBDTI通过建立明暗场光强传输正向成像模型,首次引入大角度暗场照明。因此,其可结合暗场照明下的样品信息以获取远大于物镜数值孔径(NA)所允许的细节特征,从而获得超越非相干衍射极限的空间成像分辨率。该技术可在保持原始宽视场的前提下提升成像分辨率,有望为医学诊疗、细胞培育以及微生物研究等领域,提供一双探微究因的“慧眼”。

“定量相位成像”技术:下一代无标记细胞成像的重大进展
作为生物结构与功能的基本单位,细胞的生长与分化、代谢与繁殖、运动与通讯、衰老与凋亡、遗传与进化等生命活动都同机体应答密切相关。因此,以细胞为基础的细胞生物学研究对揭示生命活性具有重要研究意义。当前,细胞生物学、临床快速诊断、药物筛选和细胞功能分析等基础医学研究逐渐发展出两大类研究需求:既可对群体活细胞进行快速无损的功能检测,又可对单细胞进行亚细胞结构和分子水平的动态功能分析。因此,如图1所示,“高通量”单细胞分析技术在生命科学领域的应用研究势在必行。
图1 细胞研究关键领域应用需求(素材来源于网络)
光学显微成像技术一直是生物医学与生命科学中的重要研究手段,也是单细胞分析的重要支撑技术之一。随着人类对生命现象本质研究的逐渐深入,新型光学显微技术层出不穷。然而由于细胞的弱吸收性,单细胞分析往往需要借助荧光成像。但现有的光学荧光显微成像方法存在两方面局限性(如图2所示):①源于荧光标记:荧光染色复杂耗时,且荧光标记物不可避免地对细胞正常生理过程产生不利影响;荧光基团存在光漂白问题,影响对细胞的长时间观察;荧光标记往往只能突出部分生物分子而难以获得细胞整体全貌。②源于光学显微成像系统:由于空间带宽积所限,提高分辨率与扩大视场往往是一对难以调和的矛盾,即无法同时满足“单细胞”与“高通量”的观测需求。
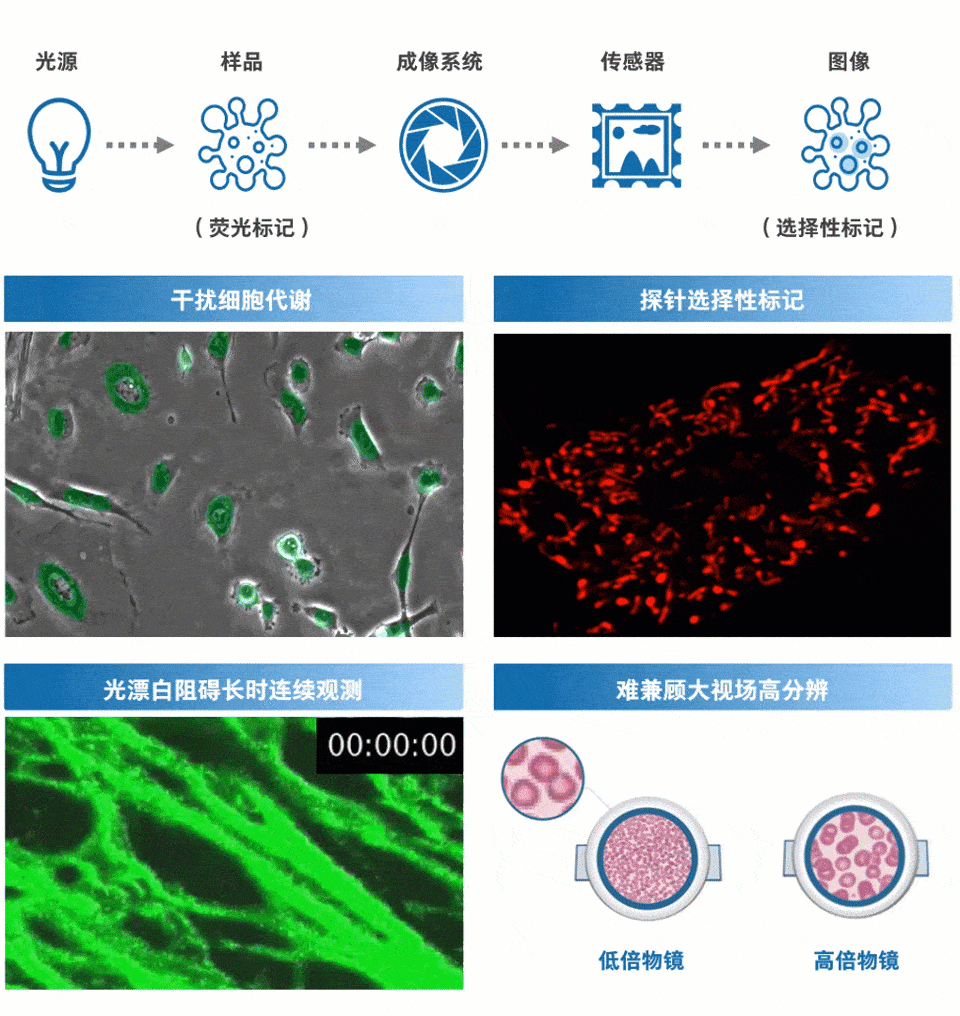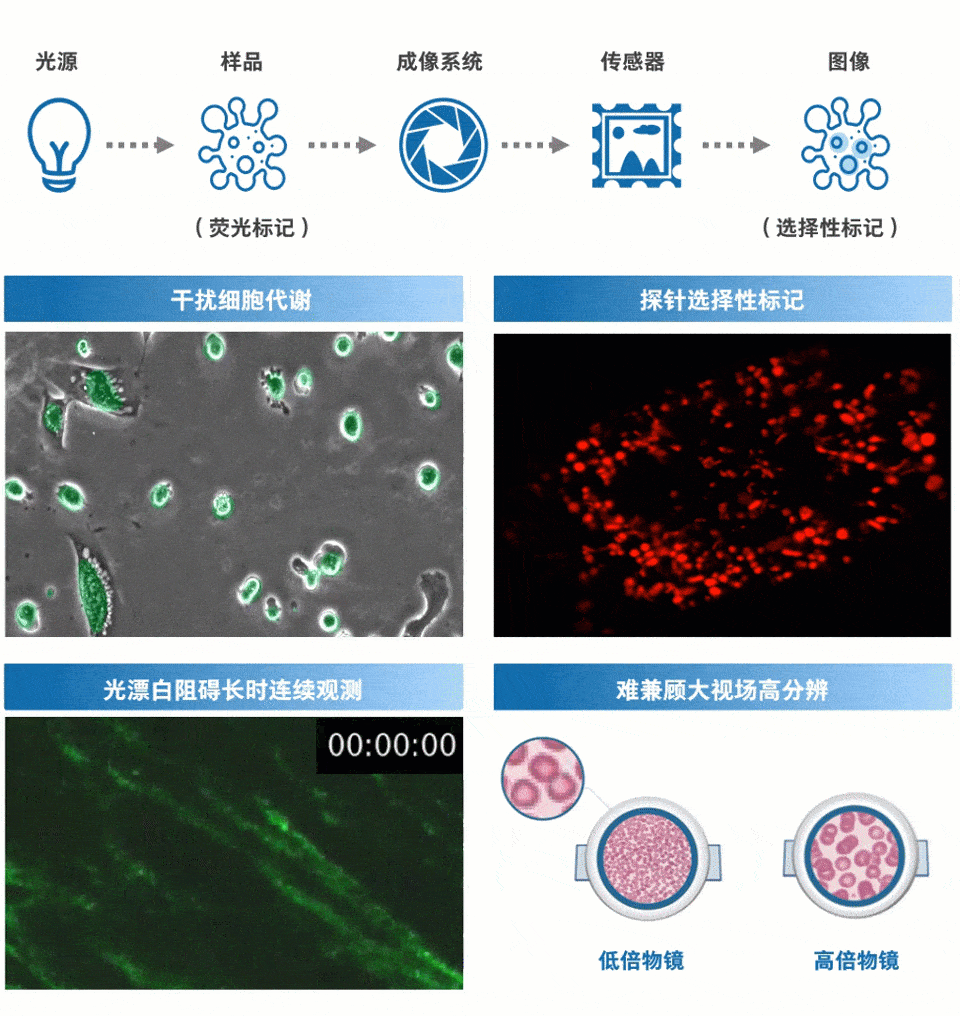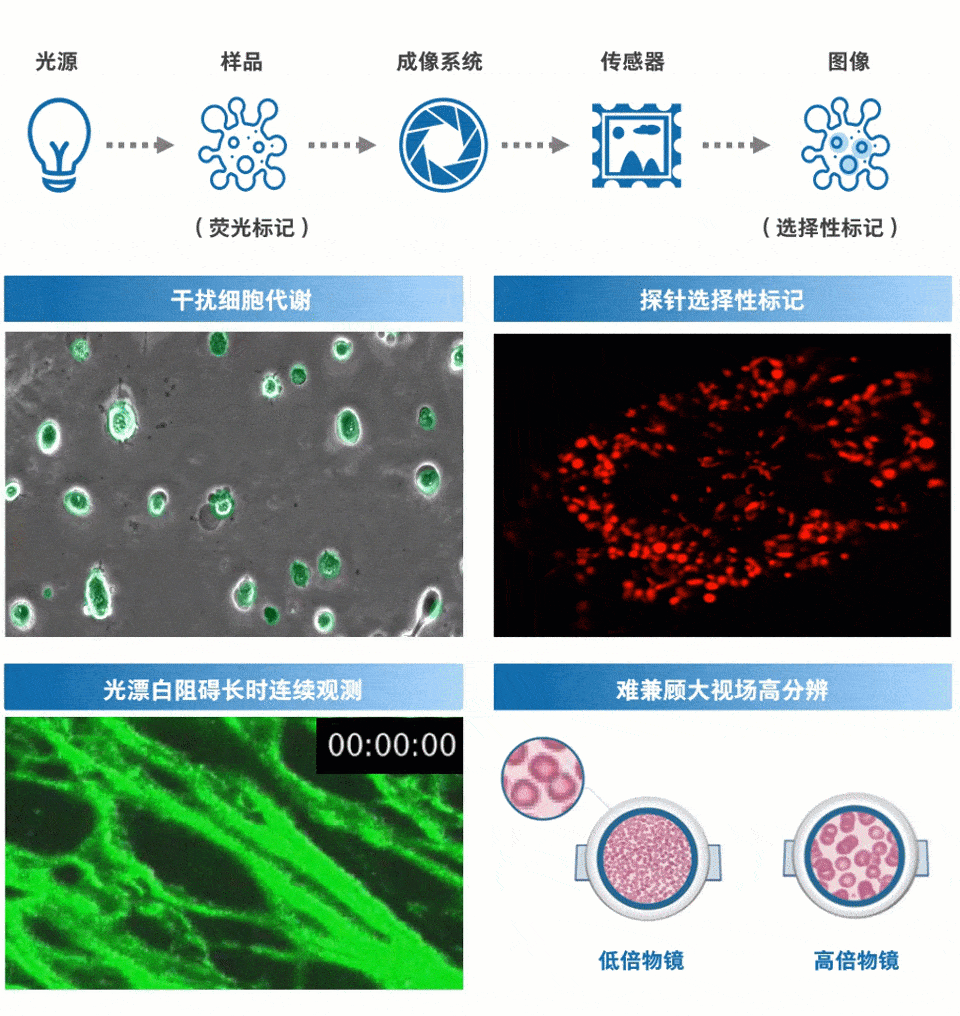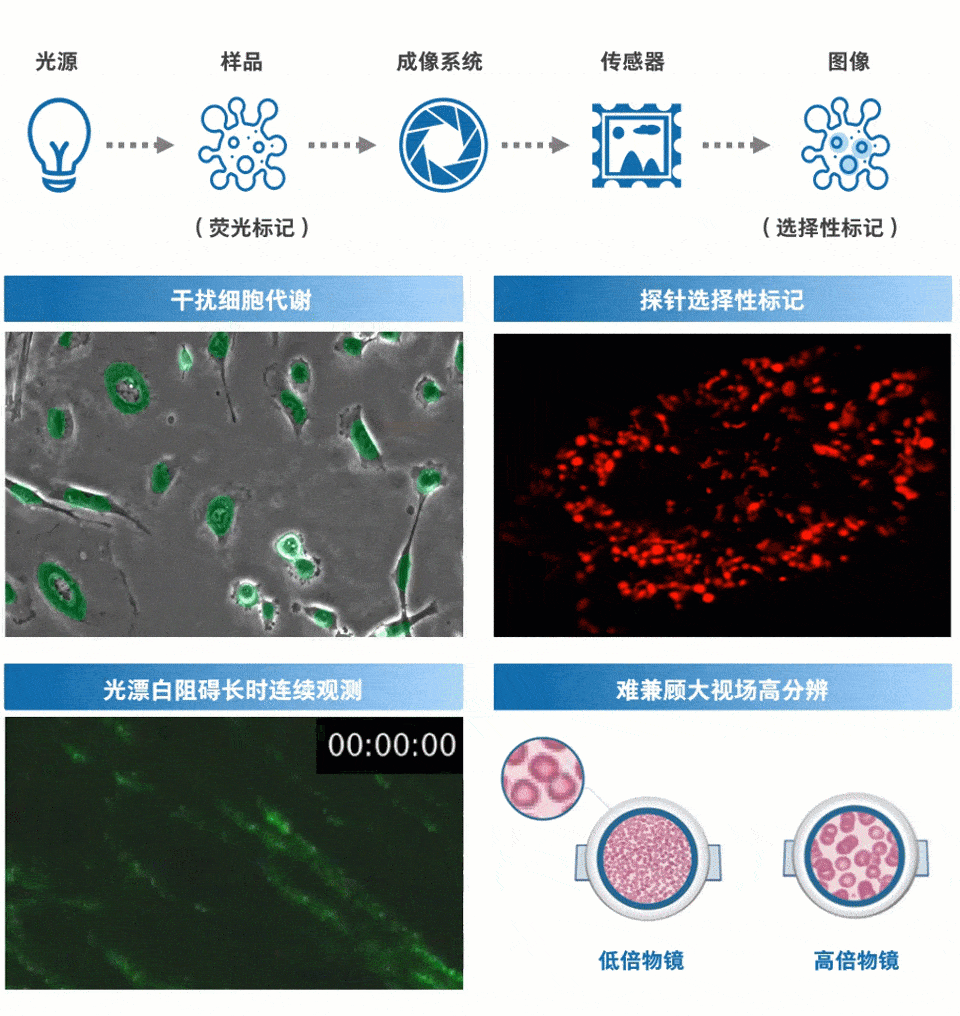
图2 现代光学显微镜的局限(部分素材来源于网络)
为解决上述因标记带来的成像难题,无标记(Label-free)显微技术为此提供了新的可能。当光通过几乎透明的物体(如细胞)时,其振幅几乎不变,而透射光的相位则包含关于样品的重要信息,如形貌与折射率分布。区别于荧光标记物这类外源性染料,相位可为高对比度成像提供合适的内源性染料。半个多世纪以来,新型无标记显微技术不断涌现,其中,“定量相位成像”技术由于其可以通过厚度及折射率系数等参数准确量化样品的信息,而被认为是“未来实现下一代无标记细胞成像的一项重大进展”。
HBDTI首次引入大角度暗场照明信息
为进一步发展“无标记、高通量”的单细胞分析技术,来自南京理工大学与香港大学的研究团队,合作提出了一种名为明暗场混合光强传输(HBDTI)的新型无标记高通量定量相位显微成像技术,将单细胞高通量成像技术提升至一个新的客观指标。
研究人员基于照明复用与合成孔径理论,建立了非线性明暗场光强传输正向成像模型,赋予了HBDTI超越非相干衍射极限的细节成像能力。与仅使用明场照明的传统光强传输方程(TIE)相位恢复方法相比,HBDTI首次引入大角度暗场照明信息,仅需基于低倍率、低数值孔径(NA)物镜即可获得具有超越非相干衍射极限空间成像分辨率的高分辨、大视场的复振幅信息。
在对USAF分辨率板、血液涂片及未染色HeLa细胞的观测实验中,该技术的高通量成像能力得到了验证:HBDTI可在约7.19 mm2的宽视场下实现488 nm半宽分辨率的高分辨成像(4倍物镜,成像分辨率达到相干衍射极限的5倍以上),成像系统的空间带宽积提升了6.25倍。
装置示意与算法流程
此研究所搭建的显微系统如图3所示,该系统为带有低NA、低倍率物镜的商用显微镜,并具备电动聚焦驱动器。对应光源被替换为可编程LED阵列,每个LED为三个单独通道以提供空间相干准单色照明,其由自主开发的电路驱动提供逻辑控制。
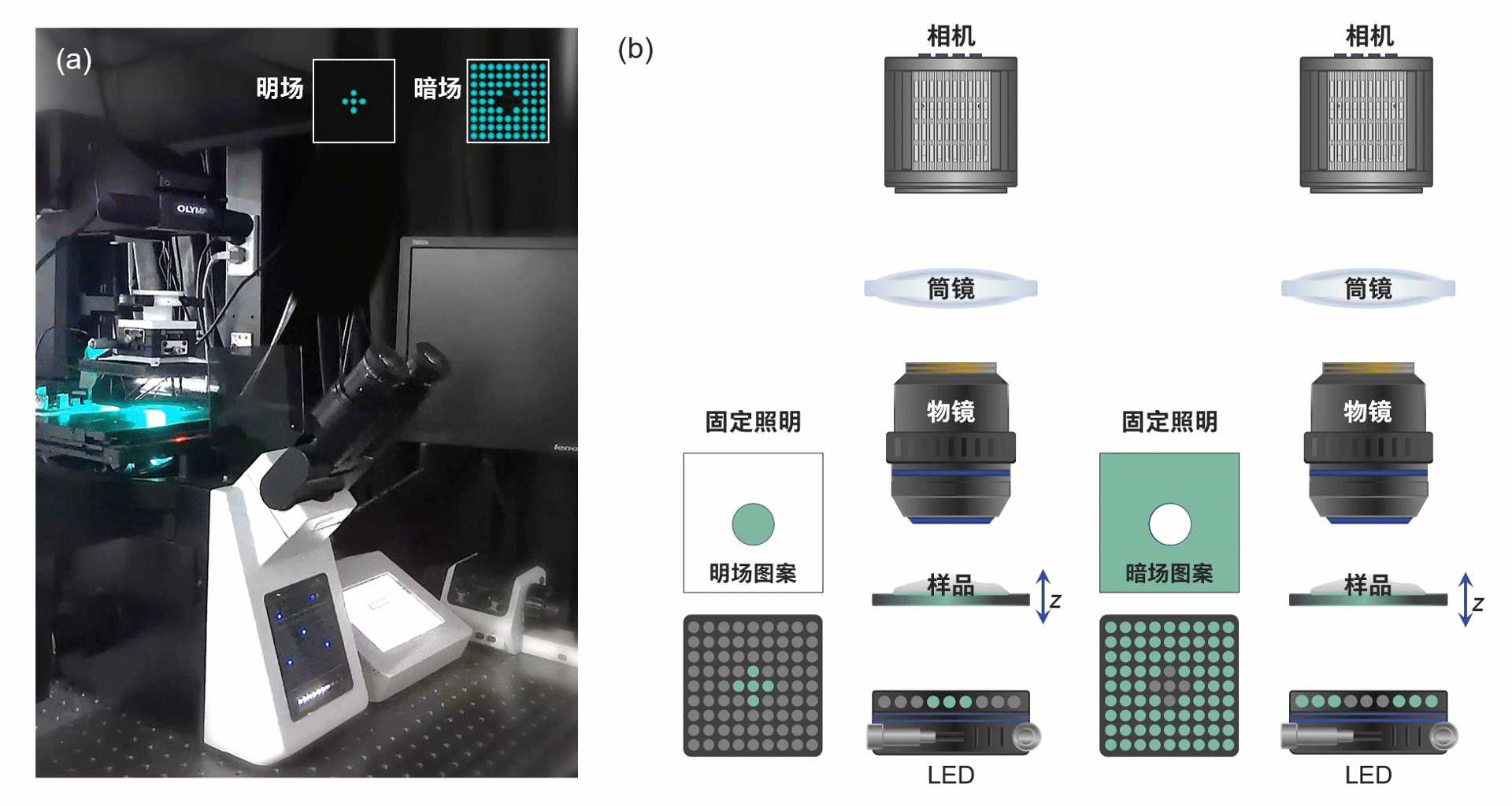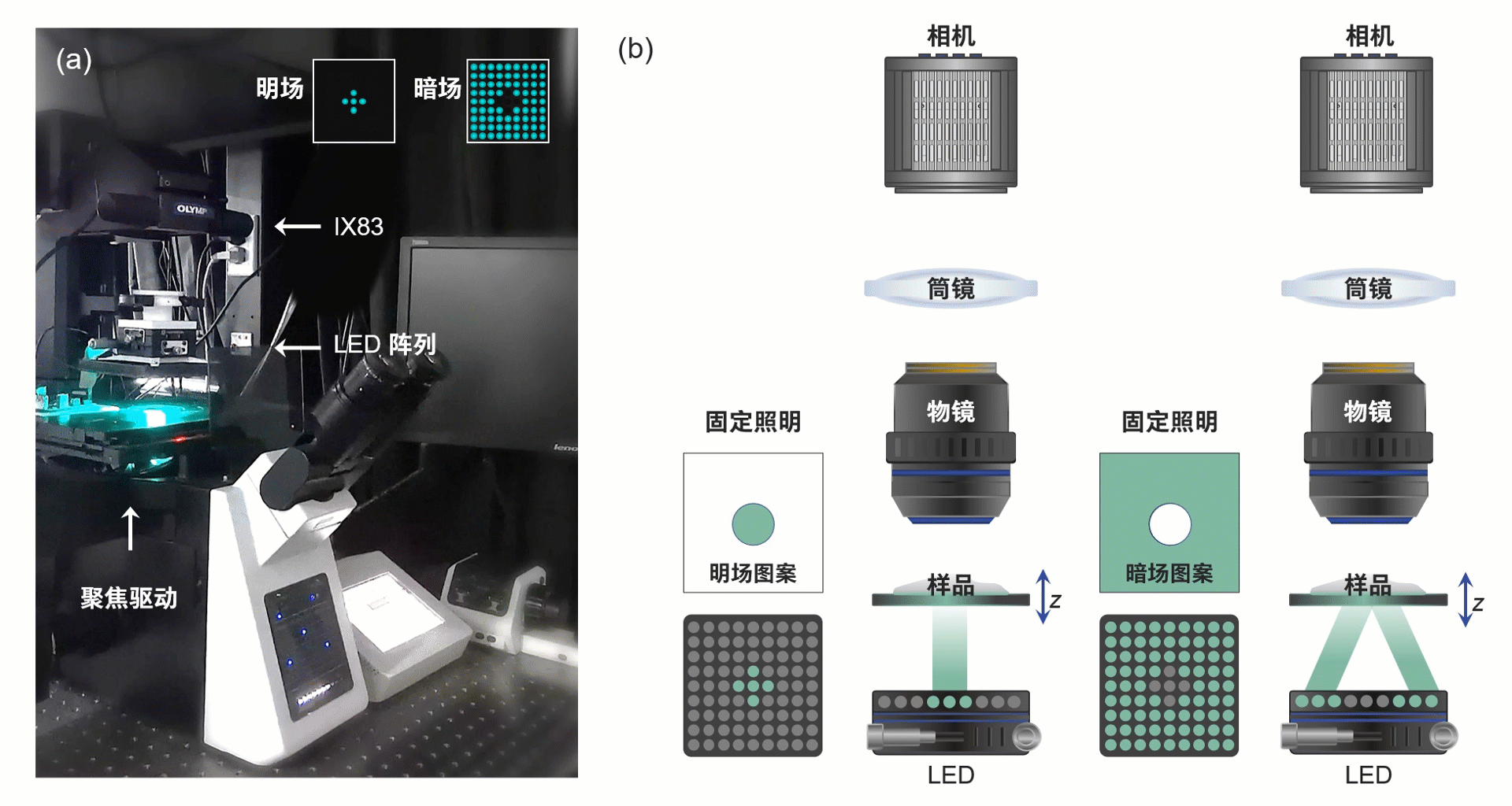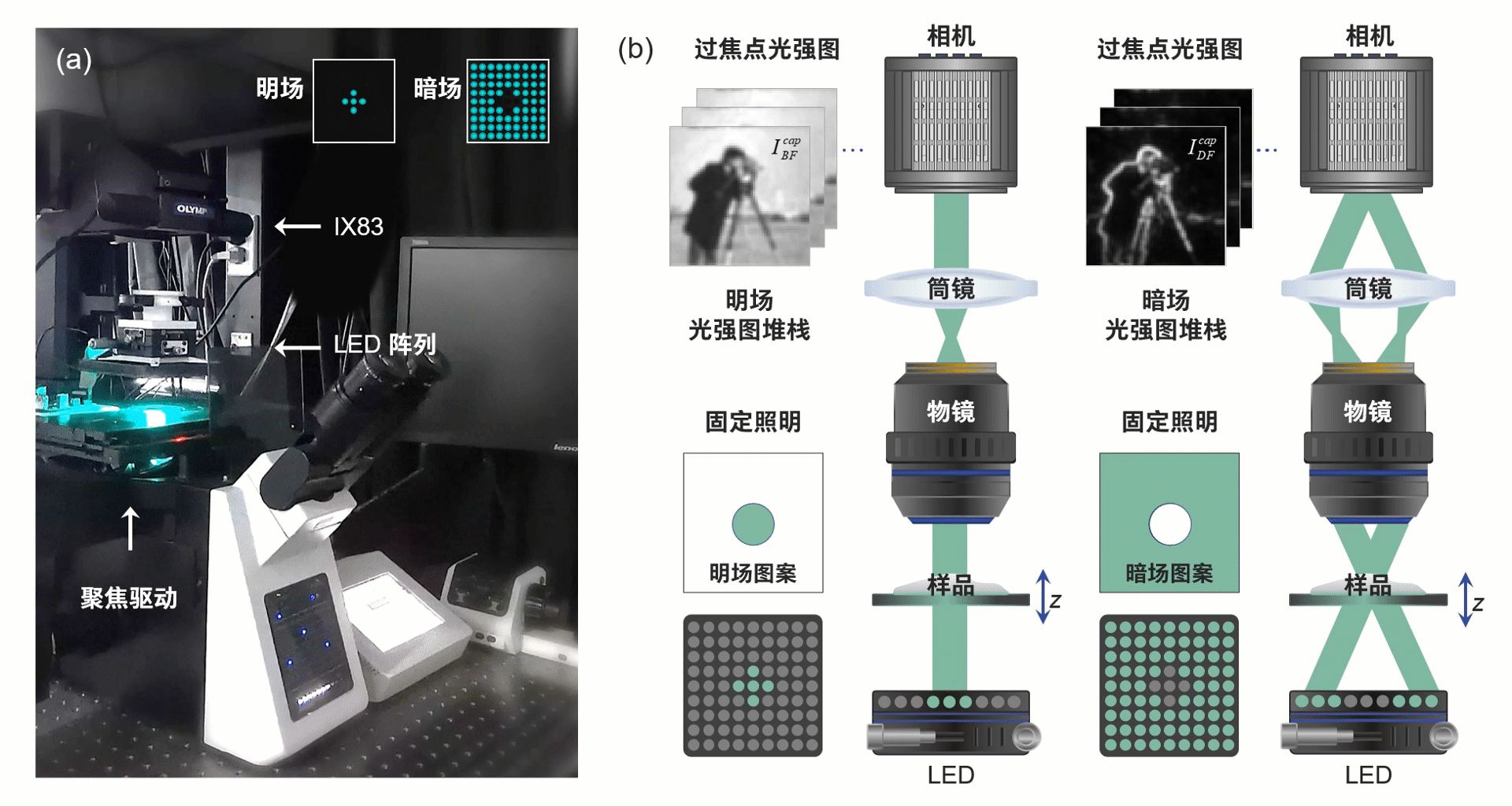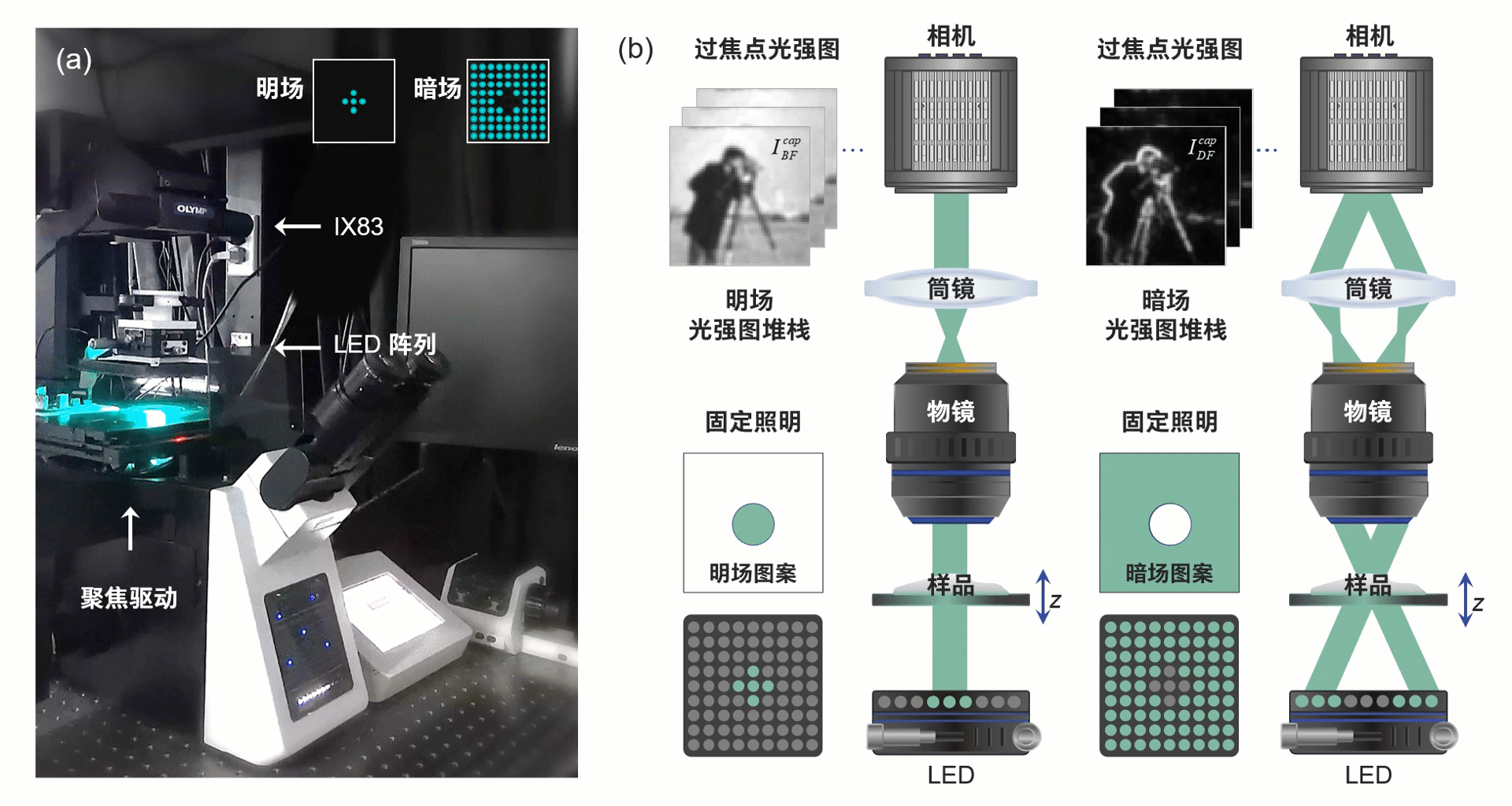
图3 系统实物图与光路示意图
为获得超越非相干衍射极限的成像分辨率,突破传统TIE技术的局限性,HBDTI技术采用了如图4所示的技术路线。它以明、暗场照明下的两组轴向强度堆栈作为输入,基于照明复用与合成孔径理论,将相干模式分解与数值传播算法相结合,实现了对光强图成像模型的正向建模。而后,HBDTI采用了正向迭代约束更新的处理框架,绕过了复杂的求解非线性逆问题所伴随而来的系列难题,在保留低倍物镜大视场的同时可恢复出具有高分辨率的复振幅成像结果。

图4 HBDTI技术路线图
HBDTI对生物样品亚微米至毫米级的高通量精确检测能力在血细胞的观测实验中得到了验证。重构结果如图5所示,HBDTI可在约7.19 mm2的大成像视场下,同时观测约八万个血细胞,红细胞的轮廓与白细胞的内部分布可被清晰分辨。
此外,为验证HBDTI对未染色生物样品的高通量成像能力,研究人员也对对未染色的HeLa细胞进行了观测对比(如图6所示)。基于HBDTI所重构的定量相位图像中可同时容纳约4000个HeLa细胞。较传统TIE技术而言,HBDTI的成像结果具有高衬度、高分辨等独特优势。
上述实验证明了HBDTI方法在细胞结构检测的高内涵分析、高通量原位观测方面所具备的潜力,并为从根本上系统揭示多细胞组织或集群中的生物组成和细胞异质性提供了可行的技术方案。

图5 血涂片的HBDTI高通量定量相位结果

图6 HeLa细胞的HBDTI高通量定量相位结果
HBDTI为生命科学研究提供新工具
HBDTI借助于暗场照明赋予了传统显微镜崭新的视野:其可在保持大视场的情况下记录高成像分辨率的图像,并具有在大规模细胞研究中描绘亚细胞结构的高通量潜力。该技术的上述优势有望为生命科学与生物医学研究等领域提供一种非侵入、高性能、低成本、定量化、简单普适的影像学分析工具,可为跨尺度细胞集群的单细胞无损检测提供高通量的定量相位信息。
未来重点需要解决的问题包括减少数据采集量与提升成像速度等。研究人员希望进一步提升成像效率,以克服显微成像系统应对复杂生物样品(如细胞集群)快速单细胞研究的关键瓶颈,并探索其在活细胞生物学、免疫肿瘤学等领域中的新应用。从而以更高的时间分辨率在更深的层次上揭示生命过程中的化学本质与规律,为探究重大疾病的起因、发展、早期诊断与有效治疗提供更可靠的科学分析依据。
最后值得一提的是,该成果得到了国内外媒体的广泛关注,并得到SPIE Newsroom的新闻推送以及多家媒体(phys.org、Newsachieve.com、AZO OPTICS等)的报道。此外,该团队将“科研成果”与“手绘艺术”有机结合,论文第一作者卢林芃大胆且富有创意地创作了一段手绘视频来形象地阐述该方法的核心思想。
视频链接:https://spie.org/news/high-throughput-computational-microscopy-imaging

图7 被SPIE Newsroom,phys.org、Newsachieve.com、AZO OPTICS等媒体报道
该工作得到了国家自然科学基金(61905115,62105151,62175109,和U21B2033);江苏省基础研究计划前沿引领专项(BK20192003);江苏省青年基金项目(BK20190445, BK20210338);中央高校科研专项资助项目(30920032101);江苏省光谱成像与智能感知重点实验室开放基金(JSGP202105)等项目的支持。




